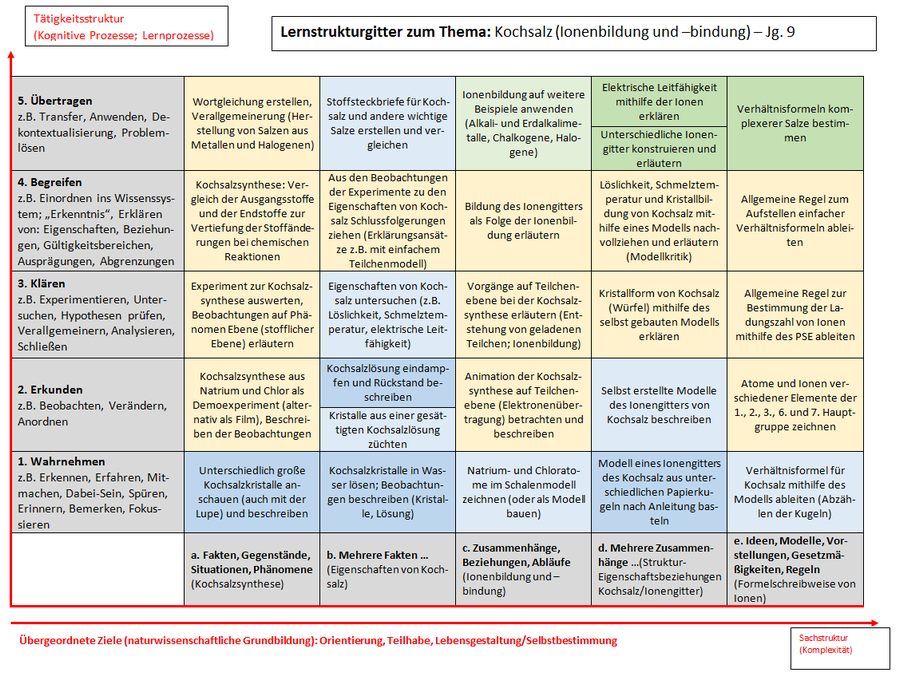
Schulentwicklung NRW - Inklusiver Fachunterricht - zu den naturwissenschaftlichen Fächern - zum Fach Chemie - Klasse 9: Kochsalz (Ionenbildung und -bindung) - „Salze – Ionenbildung und Ionenbindung“ - Darstellung einer Planung mit
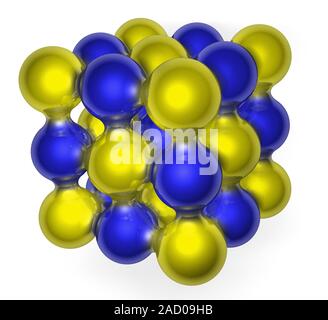
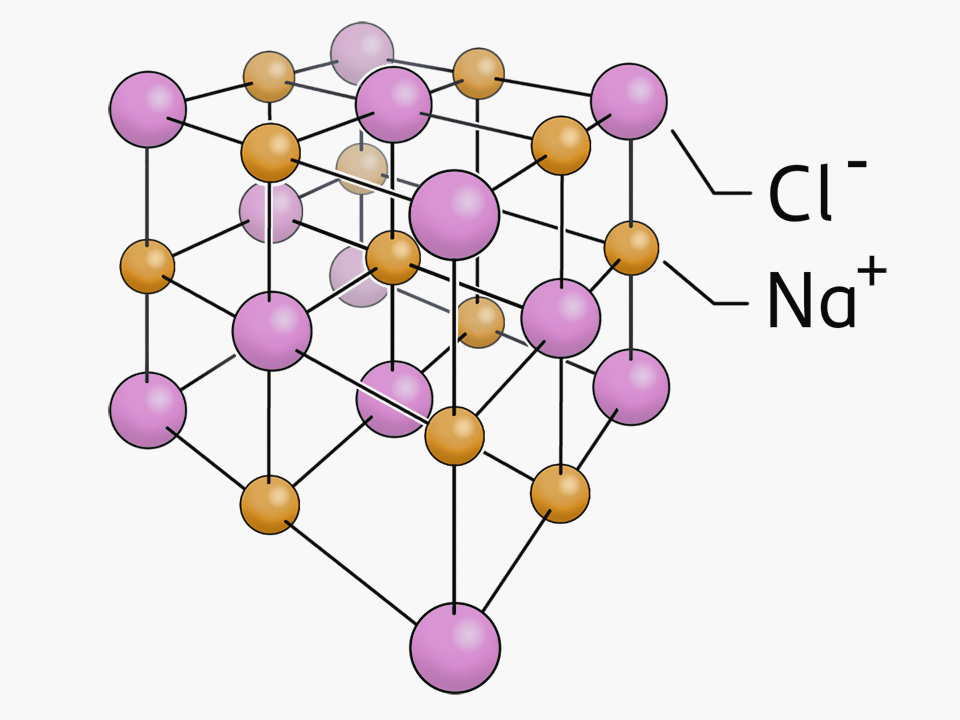
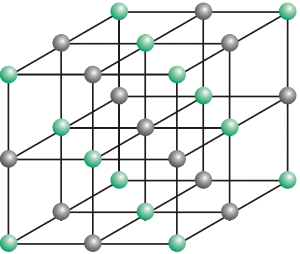
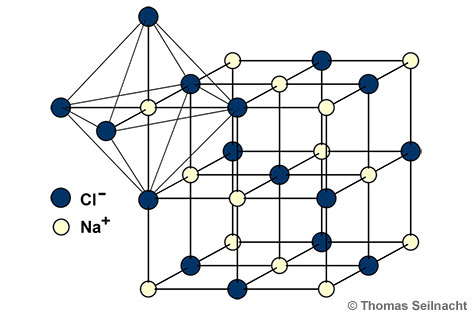
Modell der kubischen Kristallgitter von Natriumchlorid (Kochsalz). Die kubischen Kristall besteht aus einem ionisierenden Gitter von Natrium (Na+) und Chlor Stockfotografie - Alamy

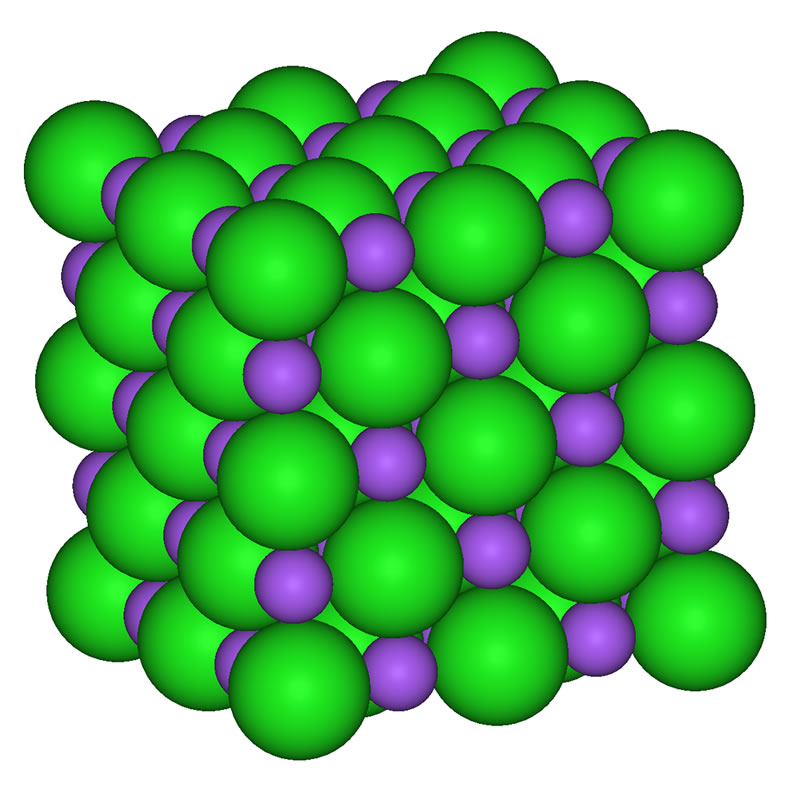
Kochsalz Kristallgittermodell, Molymod® / Gitter- und Molekülmodelle / Chemie Lehrmittel | CONATEX Lehrmittel

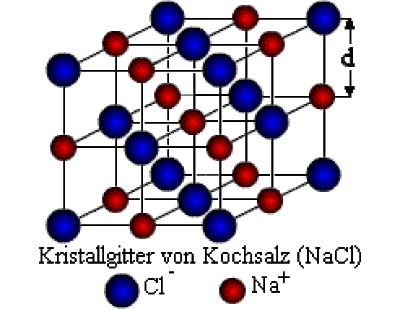
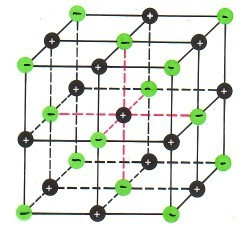


![Salze • einfach erklärt: Eigenschaften, Beispiele · [mit Video] Salze • einfach erklärt: Eigenschaften, Beispiele · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2021/09/WP_Natriumchlorid-Gitter-1024x576.jpg)







![Natriumchlorid • einfach erklärt: Verwendung, Eigenschaften · [mit Video] Natriumchlorid • einfach erklärt: Verwendung, Eigenschaften · [mit Video]](https://d3f6gjnauy613m.cloudfront.net/system/production/videos/003/410/bfe850d4531f074269837994c004b4edbb606c42/Natriumchlorid_Thumbnail.png?1639052987)